Până la 20 de noi terapii celulare și genice vor fi aprobate în fiecare an de FDA până în 2025
În ciuda prețului ridicat, terapiile genice sunt tot așteptate să fie aprobate și introduse în practica clinică curentă. Potrivit FDA, agenția de Reglementare a Medicamentelor din SUA, până în 2025, până la 20 de noi terapii celulare și genice vor fi probabil aprobate în fiecare an.
Terapiile celulare și genice ar putea salva nenumărate vieți. Sunt oameni cu cancere, cu boli rare genetice rare, cum ar fi Progeria, Spina Bifida, care ar putea beneficia de ele. Cu toate acestea, prețul mare pentru aceste tratamente ar putea împiedica accesul multor pacienți la aceste terapii, potrivit prof. dr. Kevin Doxzen, de la Universitatea de Stat din Arizona, expert în biotehnologie.
Specialistul avertizează că terapiile genice pot costa sute de mii până la milioane de dolari. Un tratament cu celule falciforme, care ar putea trata siclemia se așteaptă să fie aprobat în următorii câțiva ani.
,,Acesta ar putea costa un singur pacient în jur de 1,85 milioane de dolari. Un program Medicare ar putea plăti în jur de 30 de milioane de dolari în fiecare an, chiar dacă doar 7% dintre cei eligibili sunt tratați”, a spus prof. dr. Kevin Doxzen.
O altă terapie genică utilizată pentru tratarea atrofiei musculare spinale, o boală gravă a nervilor care cauzează atrofierea și deteriorarea mușchilor, ducând adesea la dificultăți de a se ridica, de a merge, de a respira și de a înghiți, va costa 2,1 milioane de dolari, devenind cea mai scumpă din lume.
Strângerea acestor sume mari de bani pentru aceste terapii promițătoare poate fi extrem de solicitantă pentru cei care trăiesc cu boli rare și familiile lor. Ayah Lundt, o tânără din Danemarca, diagnosticată cu atrofie musculară spinală la vârsta de 10 luni, a avut noroc să obțină suficient sprijin pentru a strânge cele 2,1 milioane de dolari pentru a beneficia de noua terapie genică, după 7 luni și jumătate obositoare de strângeri de fonduri online și licitații de la mari donatori din întreaga lume. Totuși, această abordare poate să nu fie la fel de reușită pentru alte familii.
Cum ajung aceste terapii care schimbă viața în mâinile pacienților aflați în nevoie, este o întrebare pe care și-o pun deopotrivă pacienții și medicii care-i tratează, și bineînțeles ar trebui să autoritățile să se gândească la asta.
,,Sistemul de sănătate românesc trebuie adaptat astfel încât pacienții sa aibă acces la terapii genice și celulare”, a afirmat dr. Marius Geantă, președintele Centrului pentru Inovație în Medicină, în cadrul celei de-a zecea ediții a Școlii de Boli Rare pentru Jurnaliști, organizată de Alianța Națională de Boli Rare din România.
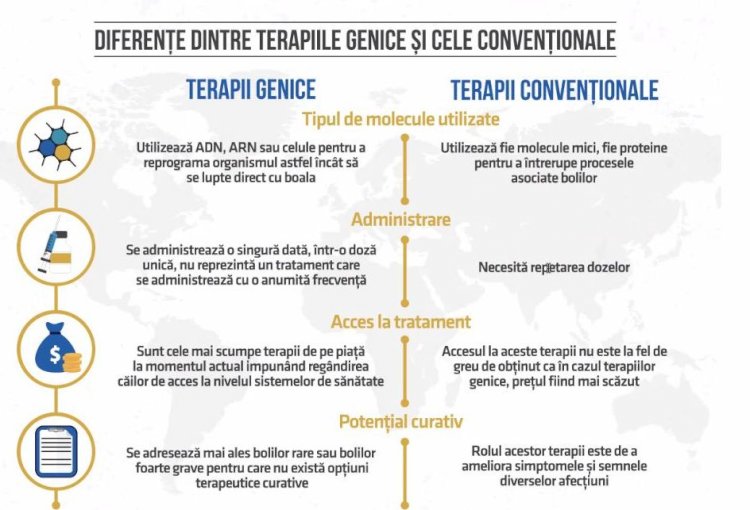
Patru mari diferențe există între terapiile genice și cele convenționale, potrivit dr. Marius Geantă, una fiind legată de accesul la ele, având în vedere că terapiile genice sunt cele mai scumpe de pe piață comparativ cu terapiile convenționale al căror preț este mult mai scăzut.
O altă diferență o reprezintă tipul de molecule utilizate. În cazul terapiilor convenționale sunt utilizate molecule mici sau proteine pentru a întrerupe procese asociate bolilor, în schimb în cazul terapiilor genice se utilizează ADN sau ARN sau celule pentru a reprograma organismul astfel încât să lupte cu boala. Modul de adminstrare diferă, în cazul terapiilor obișnuite vorbim de repetarea dozelor. În vreme ce terapiile convenționale au rolul de-a ameliora simptomele și semnele diverselor afecțiuni, terapiile genice se adresează bolilor rare, bolilor foarte grave pentru care nu există opțiuni curative.
Uniunea Europeană a aprobat deja terapii genice pentru amiotrofia spinală, pentru degenerescența retinei, avantajul acestor terapii fiind că se care se administrează o singură dată. În România deocamdată doar Institutul Fundeni este implicat în utilizarea terapiei Car-T.








